Argovia-Projekte 2017
| Projekt | Projektleiter:innen | Projektpartner:innen | |
|---|---|---|---|
| 12.01 A3EDPI - Applicability of 3D Electron Diffraction in the Pharmaceutical Industry | Dr. Tim Grüne (PSI) | Dr. Eric van Genderen (PSI) | |
| 12.04 AntibakVlies - Antibakterielle Ausstattung von Vliesmaterialien mittels e-grafting | Dr. Sonja Neuhaus (FHNW Windisch) | Dr. Joachim Köser (FHNW Muttenz) Hansjürg Härdi (Jakob Härdi AG, Oberenetfelden) | |
| 12.09 MicroSlide - Biomimetische Mikrostrukturen zur Verbesserung des Gleit- und Verschleissverhaltens | Dr. Christian Rytka (FHNW Windisch) | Prof. Dr. Ronald Holtz (FHNW Windisch) Dr. Helmut Schift (PSI) Michael Siegfried (BRUGG CABLES INDUSTRY) | |
| 12.10 MiPIS - Microfluidic Protein Isolation, Stabilization and cryo-EM Preparation for High-Resolution Structural Analysis | Dr. Thomas Braun ((Biozentrum, Univ. Basel) | Prof. Dr. Marianne Hürzeler (FHNW Muttenz) Dr. Mohamed Chami (BioEM Lab, UBAS) Michael Hennig (leadXpro, Villigen) | |
| 12.13 PlasmoRetarder - Plasmonic nanoscale retarder controlled with liquid crystals | Dr. Benjamin Gallinet (CSEM Muttenz) | Dr. Yasin Ekinci (PSI) Dr. Jean Dahdah (Rolic Technologies Ltd., Allschwil) | |
| 12.17 3D Cellophil® membrane - 3D printable nano porose Cellophil® membranes with nano hydroxyapatite gradient for tissue regeneration applications | Prof. Dr. Uwe Pieles (FHNW Muttenz) | Dr. Stefan Stübinger (HFZ, Universität Basel) Dr. Christian Geraths (CIS Pharma AG, Bubendorf) | |
12.01 A3EDPI – Strukturanalyse mit gebeugten Elektronen
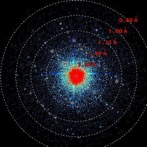
Beugungsbild eines 400 nm kleinen Kristalls des Antibiotikums Epicorazine A. (Abbildung T. Grüne, PSI).
Im Argovia-Projekt A3EDPI untersucht ein interdisziplinäres Wissenschaftler-Team vom Paul Scherrer Institut (PSI), dem C-CINA (Biozentrum, Universität Basel) sowie den Firmen Dectris AG und Crystallise! AG, ob Elektron-Nanokristallographie in der Pharmaforschung eingesetzt werden kann, um die dreidimensionale Struktur von organischen Wirkstoffen aufzuklären. Dr. Tim Grüne vom PSI leitet das Projekt, das anstrebt, die Datenerfassung sowie die -verarbeitung bei der Elektron-Nanokristallographie zu verbessern sowie die Relevanz für die pharmazeuti sche Wirkstoff-Entwicklung abzuklären.
Für die effziente Entwicklung neuer pharmazeutischer Wirkstoffe und deren Zulassung benötigen Forscher die exakte dreidimensionale Struktur der Substanzen. Liegen diese in Form einzelner Kristalle vor, lässt sich die räumliche Struktur mithilfe der Röntgenstrukturanalyse ermitteln. In vielen Fällen stehen den Wissenschaftlern jedoch nur Pulver, also Mischungen aus kristallinen Nanokörnern mit einer Grösse von nur 10 – 500 Nanometern zur Verfügung. Im Projekt A3EDPI wird nun untersucht, ob die Elektron-Nanokristallographie effizient eingesetzt werden kann, um die räumliche Struktur der Moleküle in diesen Nanokörnern aufzuklären. Dazu werden die Proben einem hochenergetischen Elektronenstrahl ausgesetzt. Da die Elektronen Welleneigenschaften besitzen, entsteht je nach Anordnung der Atome ein ganz spezifsches Beugungsbild jedes Moleküls, das Rückschlüsse über die atomare Struktur zulässt.
Erste Untersuchungen anhand einiger Modellsubstanzen haben bereits Daten von hervorragender Qualität geliefert. Nun wird das Team untersuchen, ob sich die Elektron-Nanokristallographie zu einem attraktiven Standard für die Pharma- und die chemische Industrie weiter entwickeln lässt und Anforderungen betreffend Durchsatz und Qualität für die industrielle Anwendung erreicht werden können.
12.04 AntibakVlies – weniger Bakterien auf Vliesen
In dem Argovia-Projekt AntibakVlies entwickeln Wissenschaftlerinnen und Wissenschaftler der Hochschule für Technik (FHNW), der Hochschule für Life Sciences (FHNW) und der Firma Jakob Härdi AG ein neues Verfahren, um Vliesmaterialien mit antibakteriellen und hydrophilen Eigenschaften auszustatten. Zudem arbeiten die Forscher in dem Projekt an einer effizienten Testmethode, um die antibakterielle Wirksamkeit der Vliese zu analysieren.
Momentan gibt es keine Materialien, welche die gewünschte Eigenschaftskombination aufweisen. Aus diesem Grund hat das Projektteam unter Führung von Dr. Sonja Neuhaus vom Institut für Nanotechnische Kunststoffanwendungen (INKA, Hochschule für Technik) zum Ziel, existierende Vliesmaterialien zu modifizieren.
Aus vorangegangenen Projekten wissen die Forscher, dass mittels e-grafting funktionalisierte Kunststoffoberflächen hergestellt werden können. Bei dieser Methode wird das Material zunächst mit verschiedenen Verbindungen getränkt und dann mit niederenergetischen Elektronen bestrahlt, was unter den richtigen Bedingungen zu einer kovalenten und damit dauerhaften Bindung führen kann. Im Projekt AntibakVlies werden nun verschiedene Kombinationen antibakterieller Polymere untersucht, um das Wachstum einer grossen Bandbreite von Bakterien zu verhindern.
12.09 Microslide – Bessere Gleiteigenschaften dank Schuppen

In dem Argovia-Projekt Microslide untersuchen Wissenschaftler der Fachhochschule Nordwestschweiz (FHNW) und des Paul Scherrer Instituts zusammen mit der Firma Brugg Drahtseil AG in Birr, wie sich die Gleit- und Verschleisseigenschaften von Flachriemen, die beispielsweise in Aufzügen zum Einsatz kommen, verbessern lassen. Den Forschern dient dabei die Natur als Vorbild, denn im Tierreich gibt es zahlreiche Beispiele, wie durch eine besondere Oberflächenstruktur eine gleitende Fortbewegung mit wenig Reibung unterstützt wird.
Das Wissenschaftlerteam unter Leitung von Dr. Christian Rytka vom Institut für Nanotechnische Kunststoffanwendung (INKA) plant die Oberfläche der für Hebeanwendungen verwendeten Polyurethan-Bänder mit einer schuppenartigen Oberflächenstruktur, wie sie beispielsweise Schlangen aufweisen, auszustatten. Diese Struktur soll dauerhaft die Gleiteigenschaften verbessern und daher den Verschleiss der Bänder reduzieren. In dem Projekt soll zunächst eine Prüf- und Testanlage gebaut werden, die es ermöglicht, unterschiedlich strukturierte Bänder mit den heute verwendeten zu vergleichen. Es werden dann die Eigenschaften verschiedener Oberflächenstrukturen, die durch ein Rolle-zu-Rolle Prägeverfahren eingebracht werden, auf kleinen Flächen untersucht. Schliesslich planen die Forscher die ersten Prototypen herzustellen.
12.10 MiPIS – Schnelle Aufarbeitung von Proteinen für die Analyse
Im Projekt MiPIS entwickeln Wissenschaftler des C-CINA (Biozentrum, Universität Basel) und der Hochschule für Life Sciences (FHNW) zusammen mit ihrem Industriepartner leadXpro (Villigen, AG) ein mikrofluidisches System für die Aufarbeitung und Probenvorbereitung von Proteinen, die mittels Kryo-Elektronenmikroskopie analysiert werden sollen. Dr. Thomas Braun vom C-CINA leitet das Projekt, das auf vorhergehenden, vom SNI unterstützen Arbeiten aufbaut.
Kryo-Elektronenmikroskopie (Kryo-EM) ist heute als Standardverfahren etabliert, um die atomare Struktur komplexer Proteine aufzuklären, die beispielsweise erforderlich ist, um neue Wirkstoffe für Medikamente zu entwickeln. Im Vergleich zu anderen Verfahren benötigt die Kryo-EM deutlich geringere Proteinmengen von nur einigen Nanolitern, liefert jedoch präzise Bilder in atomarer Auflösung. Die klassischen Methoden zur Aufarbeitung von Proteine werden den Anforderungen der Kryo-EM nicht immer gerecht, da sie zeitaufwendig sind, grössere Proteinmengen benötigen und teilweise die räumliche Anordnung der Proteinkomplexe zerstören. Die Wissenschaftler im Projekt MiPIS setzen nun auf die Verwendung von Mikrofluidsystemen für die Probenaufarbeitung und erhoffen sich deutliche Vorteile gegenüber den klassischen Methoden.
Am C-CINA wurde bereits ein Mikrofluid-System entwickelt, mit dem Proben direkt auf einen für die Elektronenmikroskopie benötigen Objektträger platziert werden. Innerhalb des Argovia-Projektes MiPIS soll dieses System nun weiterentwickelt werden, sodass Proteine in dem System innerhalb von zwei Stunden gereinigt, stabilisiert und unter Beibehaltung ihrer räumlichen Struktur für die Kryo-EM-Analyse vorbereitet werden können.
12.13 PlasmoRetarder – Elektrisch steuerbare Farben

Im Projekt PlasmoRetarder planen die Wissenschaftler einen Phasenverzögerer zu entwickeln und die emittierte Farbe elektrisch zu steuern.
Im Nano-Argovia-Projekt «PlasmoRetarder» entwickeln Wissenschaftler vom CSEM in Muttenz und dem Paul Scherrer Institut (Villigen, AG) zusammen mit ihrem Industriepartner Rolic Technologies Ltd (Allschwil, BL) einen plasmonischen Phasenverzögerer, der für Displays in der Sensorik oder zur Abbildung angewendet werden kann. Dr. Benjamin Gallinet vom CSEM Muttenz leitet das Projekt. An den Oberflächen von nanostrukturierten Metallen können Elektronen zu kollektiven Schwingungen, die Oberflächenplasmonen genannt werden, angeregt werden. Derartige plasmonische Nanostrukturen sind in der Lage, Licht bis in den Nanobereich zu fokussieren, sowie die Farbe, Phase und Polarisation des Lichts zu beeinflussen. So können derartige Strukturen beispielsweise als Farbfilter mit hervorragender Auflösung und einem breiten Einsatzbereich verwendet werden. Im Projekt PlasmoRetarder planen die Wissenschaftler nun einen steuerbaren Phasenverzögerer zu entwickeln, zu charakterisieren und zu optimieren. Sie stellen dazu Nanostrukturen mit Abmessungen von bis zu 100 Nanometern her und entwickeln einen optimalen Beschichtungsprozess mit Metallen. Mithilfe von Flüssigkristallen möchte das Team die vom Phasenverzögerer emittierte Farbe elektrisch steuern. In einem zweiten Schritt soll der entwickelte Phasenverzögerer dann in ein Gerät eingebaut werden, um zu belegen, dass der Einsatz der Technologie in optoelektronischen Geräten eine Zukunft haben kann.
12.17 3D Cellophil® Membran – Patientenspezifisch und den Bedingungen im Mund angepasst
Das Nano-Argovia Projekt «3D Cellophil®» hat zum Ziel neuartige, nanostrukturierte Implantate zu entwickeln, welche die Regeneration von Knochen und Weichteilen im Kiefer- und Mundbereich unterstützen und patientenspezifisch durch 3D-Druck hergestellt werden können. Professor Uwe Pieles von der Hochschule für Life Sciences an der Fachhochschule Nordwestschweiz ist Projektleiter des Teams, zu dem Wissenschaftler der FHNW, des Hightech-Forschungs-Zentrums für Mund-Kiefer-Gesichtschirugie des Universitätsspitals Basel sowie der Firma CIS Pharma AG (Bubendorf, BL) gehören.
Die Wissenschaftler entwickeln in dem Projekt eine dreischichtige Polymer-Membran, basierend auf der von CIS Pharma entwickelten Cellophil®-Technologie. Cellophil® ist eine Mischung verschiedener natürlicher Aminosäuren, die über ein Acryl-Rückgrat verbunden sind und sich durch eine sehr gute Biokompatibilität auszeichnen. Die Polymere werden mit vernetzenden Substanzen gemischt. Je nach Menge führt dies nach Bestrahlung mit UV-Licht zu unterschiedlich porösen Membranen. Die Wissenschaftler machen sich dies zunutze und statten die drei Schichten des Implantats mit unterschiedlichen Eigenschaften aus. Die beiden äusseren Schichten sind porös und unterstützen die Besiedlung mit den knochenaufbauenden Osteoblasten auf den Knochen zugewandten Flächen und mit Fibroblasten auf der Seite, die mit der Schleimhaut in Kontakt steht. Die mittlere Schicht der Membran hat einen höheren Gehalt an vernetzenden Substanzen und ist daher weniger durchlässig für die Zellen. Dies soll verhindern, dass die schnell wachsenden Fibroblasten die sich langsamer vermehrenden Osteoblasten überwuchern und die Knochenneubildung hemmen. Die zwei den Zellen zugewandten äusseren Schichten weisen zudem verschiedene Konzentrationen von aktiven Substanzen auf, die ganz spezifisch das Wachstum und die Differenzierung von Osteoblasten respektive Fibroblasten unterstützen. Obwohl die drei Schichten unterschiedlich aufgebaut sind, können sie in einem Schritt und spezifisch für den jeweiligen Patienten angepasst gedruckt werden.
